Le CBD et le THC partagent exactement la même formule moléculaire, C21H30O2, contenant vingt et un atomes de carbone, trente d’hydrogène et deux d’oxygène.
Leur masse moléculaire est pratiquement identique au THC et au CBD ayant des masses de 314,469 g / mol 314,464 g / mol, respectivement.
Propriétés chimiques et physiques de la molécule de THC
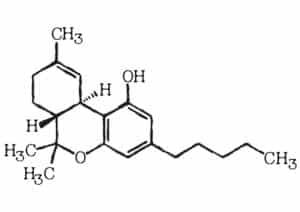
Le tétrahydrocannabinol, également connu sous le nom de dronabinol, est la principale substance psychoactive présente dans la plante de cannabis.
Il a été isolé par Raphael Mechoulam, Yechiel Gaoni et Habib Edery de l’Institut Weizmann à Rehovot, Israël en 1964.
Sous sa forme pure, c’est un solide vitreux lorsqu’il est froid, et devient visqueux et collant s’il est chauffé. Terpénoïde aromatique, le THC a une très faible solubilité dans l’eau, mais une bonne solubilité dans la plupart des solvants organiques tels que le butane ou l’hexane.
Comme c’est le cas avec la nicotine et la caféine, le rôle du THC dans le cannabis, semble-t-il, est de protéger la plante des herbivores ou des agents pathogènes.
Le THC possède également de hautes propriétés d’absorption UV-B (280-315 nm), protégeant la plante contre les:
Pharmacologie
Les actions pharmacologiques de la molécule de THC résultent de sa liaison au récepteur cannabinoïde CB1, situé dans le cerveau.
La présence de ces récepteurs spécialisés dans le cerveau impliquait pour les chercheurs que les cannabinoïdes endogènes sont fabriqués par le corps, alors la recherche a commencé pour une substance normalement fabriquée dans le cerveau qui se lie à ces récepteurs, le soi-disant ligand naturel ou agoniste, conduisant à la découverte éventuelle de l’anandamide, du 2-arachidonyl glycéride (2-AG) et d’autres composés apparentés.
Cette histoire ressemble à la découverte des opiacés endogènes (endorphines, enképhalines et dynorphine), après la prise de conscience que la morphine et d’autres opiacés se lient à des récepteurs spécifiques dans le cerveau.
De plus, il a été montré que les cannabinoïdes, par un mécanisme inconnu, activent les voies opioïdes endogènes via le récepteur opioïde, précipitant une libération de dopamine dans le noyau accumbens.
Les effets du médicament peuvent être supprimés par l’antagoniste des récepteurs cannabinoïdes CB1 rimonabant (SR141716A) ou, intéressant à noter, les antagonistes des récepteurs opioïdes (bloqueurs d’opioïdes), la naloxone et la naloxonazine.
Le mécanisme de transmission synaptique endocannabinoïde est compris par les événements suivants: Une transmission excitatrice du neurotransmetteur glutamate provoque un afflux d’ions calcium dans le neurone post-synaptique.
Par un mécanisme encore mal compris, la présence de calcium post-synaptique induit la production d’endocannabinoïdes dans le neurone post-synaptique.
Ces endocannabinoïdes (comme l’anandamide) sont libérés dans la fente synaptique.
Une fois dans la fente synaptique, la liaison se produit au niveau des récepteurs cannabinoïdes présents dans les neurones pré-synaptiques où ils peuvent ensuite moduler la neurotransmission de manière pré-synaptique.
Cette forme de neurotransmission est appelée transmission rétrograde, car le signal est transporté dans la direction opposée de la propagation orthodoxe; il donne un aperçu intéressant de la neurotransmission,
La molécule de THC a des effets analgésiques qui, même à faibles doses, provoquent un high, conduisant ainsi au fait que le cannabis médical peut être utilisé pour traiter la douleur.
Le mécanisme des effets analgésiques causés directement par le THC ou d’autres agonistes cannabinoïdes n’est pas entièrement élucidé.
D’autres effets incluent la relaxation; euphorie; altération de la perception de l’espace-temps; altération des sens visuels, auditifs et olfactifs; désorientation; fatigue; et la stimulation de l’appétit liée à l’activité des récepteurs CB1 dans le système nerveux central.
Le mécanisme de stimulation de l’appétit chez les sujets est quelque peu compris et expliqué par un axe gastro-hypothalamique.
L’activité CB1 dans les centres de la faim dans l’hypothalamus augmente l’appétence des aliments lorsque les niveaux d’une hormone de la faim, la ghréline, augmentent à mesure que les aliments pénètrent dans l’estomac.
Après que le chyme soit passé dans le duodénum, des hormones de signalisation telles que la cholécystokinine et la leptine sont libérées, entraînant une réduction de la vidange gastrique et la transmission des signaux de satiété à l’hypothalamus, respectivement.
L’activité cannabinoïde est réduite par les signaux de satiété induits par la libération de leptine.
Il a également des propriétés anti-émétiques et peut également réduire l’agressivité chez certains sujets.
Le THC a un métabolite actif, le 11-Hydroxy-THC, qui peut également jouer un rôle dans les effets analgésiques et récréatifs de l’herbe.
Toxicité

Selon le Merck Index, 12e édition, le THC a une DL50 de 1270 mg / kg (rats mâles) et de 730 mg / kg (rats femelles) administrés par voie orale dissous dans de l’huile de sésame.
Si cela était étendu à un humain adulte, la DL50 serait entre environ 86 g et 50 g pour un homme ou une femme de 68 kg (150 lb), respectivement.
Cela équivaudrait à 1-1,8 kg de cannabis avec une teneur en THC de 5% (en moyenne) pris par voie orale.
La valeur DL50 pour les rats par inhalation de THC est de 42 mg / kg de poids corporel.
Il est important de noter, cependant, que la toxicité sur les animaux ne correspond pas nécessairement à la toxicité humaine.
La distribution des récepteurs du THC dans le système nerveux central du rat est différente de celle des humains, ce qui signifie qu’il existe une possibilité significative que la toxicité chez l’homme diffère des études publiées sur la DL50 chez l’animal.
L’absorption est limitée par les lipides sériques, qui peuvent devenir saturés de THC, ainsi la solubilité inhérente peut atténuer la toxicité.
Des études sur la distribution des récepteurs cannabinoïdes dans le cerveau expliquent pourquoi la toxicité du THC est si faible (c’est-à-dire que la DL50 du composé est si grande):
les parties du cerveau qui contrôlent les fonctions vitales telles que la respiration n’ont pas beaucoup de récepteurs, donc elles sont relativement peu affectés, même par des doses plus importantes que celles qui ne pourraient jamais être ingérées dans des conditions normales.
Recherche
Un certain nombre d’études indiquent que le THC peut apporter des avantages médicaux aux patients atteints de cancer et de sida en augmentant l’appétit et en diminuant les nausées.
Il a été démontré qu’il aide certains patients atteints de glaucome en réduisant la pression à l’intérieur de l’œil et est utilisé sous forme de cannabis par un certain nombre de patients atteints de sclérose en plaques pour soulager les spasmes et la douleur associés à leur maladie.
De nouvelles preuves scientifiques montrent que la molécule de THC peut prévenir la maladie d’Alzheimer en neutralisant l’activation de la microglie et en induisant ainsi l’inflammation de la microglie se liant à la protéine amyloïde.
Certaines études affirment également une variété d’effets négatifs associés à une utilisation constante et à long terme, y compris une perte de mémoire à court terme.
D’autres études ont réfuté cela par des preuves d’IRM d’utilisateurs à long terme montrant peu ou pas de différence avec les IRM du groupe témoin non-utilisant.
Bien que utilisant la tomographie par émission de positons (TEP), au moins une étude affirme avoir observé une fonction cérébrale altérée liée à la mémoire chez les utilisateurs de marijuana.
Les effets à long terme du THC sur les humains ont été contestés parce que son statut de drogue illégale rend la recherche difficile.
Des recherches préliminaires sur les molécules de THC synthétiques ont été menées sur des patients atteints du syndrome de Tourette, avec des résultats suggérant que cela pourrait aider à réduire les tics nerveux et les pulsions de manière significative.
Et Des études animales ont suggéré que le marinol et la nicotine pourraient être utilisés comme un complément efficace aux médicaments neuroleptiques dans le traitement du TS.
Puis Des recherches sur douze patients ont montré que Marinol réduisait les tics sans effets indésirables significatifs.
Une étude contrôlée de six semaines sur 24 patients a montré que les patients prenant Marinol présentaient une réduction significative de la gravité des tics sans effets indésirables graves.
Sept patients ont abandonné ou ont dû être exclus de l’étude, un en raison d’effets secondaires indésirables.
Une réduction plus significative de la sévérité des tics a été rapportée avec un traitement plus long.
Aucun effet néfaste sur le fonctionnement cognitif et une tendance à l’amélioration du fonctionnement cognitif n’ont été signalés pendant et après le traitement.
L’utilité du marinol comme traitement du TS ne peut être déterminée tant que des études contrôlées plus longues sur des échantillons plus grands ne sont pas entreprises.
Des recherches récentes ont montré que de nombreux effets secondaires indésirables, généralement connus sous le nom de stéréotype «stoner», ne résistent pas à la méthode scientifique.
Des études récentes avec des cannabinoïdes synthétiques montrent que l’activation des récepteurs CB1 peut faciliter la neurogénération, ainsi que la neuroprotection, et peut même aider à prévenir la dégradation neurale naturelle des maladies neurodégénératives telles que
- la SEP,
- la maladie de Parkinson
- et la maladie d’Alzheimer;
Cependant, la neurogénération ne s’est produite que chez le rat en raison de l’introduction d’un isomère optique du THC, et non du THC lui-même.
Ceci, combiné à la recherche sur le récepteur CB2 (dans tout le système immunitaire), a donné plus de soutien à la marijuana médicale.
Dans des expériences in vitro, le THC à des concentrations extrêmement élevées, qui ne pouvaient pas être atteintes avec des doses couramment consommées, a provoqué une inhibition de la formation de plaques, la cause de la maladie d’Alzheimer, mieux que les médicaments actuellement approuvés.
Le THC peut également être un traitement anticancéreux efficace, avec des études montrant une réduction de la tumeur chez les souris, menées en 1975.
Le 28 juillet 2007, la revue médicale britannique The Lancet a publié une étude qui indique que les consommateurs de cannabis ont, en moyenne, un risque 41% plus élevé de développer une psychose que les non-utilisateurs.
Le risque était le plus prononcé dans les cas avec un risque existant de trouble psychotique, et aurait augmenté jusqu’à 200% pour les utilisateurs les plus fréquents.
Un risque de développer une psychose 41% plus élevé que les non-utilisateurs.
Le risque était le plus prononcé dans les cas avec un risque existant de trouble psychotique, et aurait augmenté jusqu’à 200% pour les utilisateurs les plus fréquents.
Un risque de développer une psychose 41% plus élevé que les non-utilisateurs.
Le risque était le plus prononcé dans les cas avec un risque existant de trouble psychotique, et aurait augmenté jusqu’à 200% pour les utilisateurs les plus fréquents.
Des recherches récentes ont également montré une corrélation entre la consommation de cannabis et une fonction cognitive accrue chez les patients schizophrènes.
Une étude de deux ans dans laquelle des rats et des souris ont été gavés de tétrahydrocannabinol dissous dans de l’huile de maïs a montré une masse corporelle réduite, des taux de survie améliorés et une diminution de l’incidence des tumeurs dans plusieurs sites, principalement des organes sous contrôle hormonal.
Elle a également provoqué une atrophie testiculaire et une hypoplasie utérine et ovarienne, ainsi qu’une hyperactivité et des convulsions immédiatement après l’administration.
Chez la souris, de faibles doses de? 9-THC réduisent la progression de l’athérosclérose.
Biosynthèse
Dans la plante de cannabis, le THC se présente principalement sous forme d’acide tétrahydrocannabinol carboxylique (THC-COOH).
La condensation enzymatique de pyrophosphate de géranyle et d’acide olivétolique donne de l’acide cannabigérolique qui est cyclisé par l’enzyme THC acide synthase pour donner THC-COOH.
Le chauffage décarboxyle l’acide en THC.
Métabolisme
Le THC est principalement métabolisé en 11-OH-THC (11-hydroxy-THC) par le corps humain.
Ce métabolite est encore psychoactif et est ensuite oxydé en 11-nor-9-carboxy-THC (THC-COOH).
Chez l’homme et l’animal, plus de 100 métabolites ont pu être identifiés, mais le 11-OH-THC et le THC-COOH sont les métabolites dominants.
Le métabolisme se produit principalement dans le foie par les enzymes du cytochrome P450 CYP2C9, CYP2C19 et CYP3A4.
Plus de 55% du THC sont excrétés dans les fèces et ~ 20% dans l’urine.
Le principal métabolite dans l’urine est l’ester d’acide glucuronique et de THC-COOH et de THC-COOH libre.
Dans les fèces, le 11-OH-THC a été détecté principalement.
Molécule de THC synthétique

Le THC synthétique, également connu sous le nom de substance dronabinol, est disponible en tant que médicament d’ordonnance (sous le nom commercial Marinol) dans plusieurs pays, dont les États-Unis et l’Allemagne.
Aux États-Unis, le Marinol est un médicament de l’annexe III, disponible sur ordonnance, considéré comme non narcotique et à faible risque de dépendance physique ou mentale.
Les efforts pour obtenir le report du cannabis comme analogue à Marinol n’ont pas réussi jusqu’à présent, bien qu’une pétition de 2002 ait été acceptée par la DEA.
À la suite du rééchelonnement du Marinol du Tableau II au Tableau III, les recharges sont désormais autorisées pour cette substance.
Marinol a été approuvé par la FDA dans le traitement de l’anorexie chez les patients atteints du SIDA, ainsi que pour les nausées et vomissements réfractaires des patients sous chimiothérapie.
Un analogue du dronabinol, le nabilone, est disponible dans le commerce au Canada sous le nom commercial Cesamet, fabriqué par Valeant.
Cesamet a également reçu l’approbation de la FDA pour une disponibilité future aux États-Unis et est un médicament de l’annexe II.
En avril 2005, les autorités canadiennes ont approuvé la commercialisation du Sativex, un spray buccal pour la sclérose en plaques destiné à soulager la douleur.
Sativex contient du tétrahydrocannabinol en association avec du cannabidiol.
Il est commercialisé au Canada par GW Pharmaceuticals, étant le premier médicament d’ordonnance à base de cannabis au monde.
Trouvez ici: THC et CBD : Quelle est la Différence?










